Seitenpfad:
- Presse
- Pressemeldungen 2013
- 04.11.2013 Das Stickstoff-Puzzle in den Ozeanen
04.11.2013 Das Stickstoff-Puzzle in den Ozeanen
Das Stickstoff-Puzzle in den Ozeanen
Anammox-Stickstoff-Isotopeneffekte entschlüsselt
Ein Wissenschaftlerteam des Max-Planck-Instituts für Marine Mikrobiologie, der Universität Basel und der Radboud Universität Nijmegen hat entscheidende Details eines wichtigen mikrobiellen Prozesses aufgedeckt und leistet damit einen großen Beitrag zum Verständnis der Stickstoffbilanz in den Weltmeeren. Sie berichten darüber in der Fachzeitschrift Proceedings of the National Academy of Sciences, USA.
Jedes Lebewesen braucht Stickstoff zum Leben und Wachsen
Viele Organismen haben nicht die Fähigkeit, lebensnotwendigen Stickstoff direkt aus dem molekularen Stickstoff zu nutzen, der als gasförmiges N<sub>2 </sub> in der Atmosphäre vorkommt. Sie haben in ihren Zellen nicht die entsprechenden Werkzeuge zur Stickstoff-Fixierung und sind deshalb auf Stickstoffverbindungen wie Ammonium, Nitrit und Nitrat angewiesen, die von den sogenannten Stickstoff-fixierenden Organismen kommen. In der Natur reguliert daher die biologische Verfügbarkeit von fixiertem Stickstoff häufig die Primärproduktion. Deshalb sind Düngemittel oft reich an Stickstoffverbindungen.
Es gibt in der Umwelt eine Reihe von anderen mikrobiellen Prozessen, die fixierten Stickstoff zur Energiegewinnung nutzen und wieder zu gasförmigem molekularen Stickstoff (N<sub>2 </sub>) umwandeln. Wissenschaftler sprechen hier von einem Verlust an fixiertem Stickstoff, weil dabei der jeweilige Lebensraum wichtige Stickstoffverbindungen verliert und so die Primärproduktion eingeschränkt wird.
Die Prozesse, die zum Stickstoffverlust führen, laufen in verschiedenen Mikroorganismen ab, manche reduzieren Nitrat und Nitrit, manche oxidieren Ammonium. Andere Bakterien nutzen Nitrit und Ammonium, um daraus molekularen Stickstoff zu bilden: Diese anaerobe Oxidation von Ammonium ist unter dem Begriff Anammox bekannt.
Stickstoffverluste sind besonders stark in den Meeresgebieten ausgeprägt, in denen der im Wasser gelöste Sauerstoff fast komplett verbraucht wurde. Diese Zonen werden als Oxygen Minimum Zones (OMZ) bezeichnet. Wissenschaftliche Studien lassen befürchten, dass sich diese OMZ aufgrund des Klimawandels weiter ausbreiten werden. Das könnte zu weitreichenden Konsequenzen bei den Stickstoffverlusten und damit bei der Primärproduktion in den Ozeanen führen. Deshalb ist es wichtig zu wissen, welcher mikrobielle Prozess wie stark zu den gesamten Stickstoffverlusten beiträgt und wo dieser innerhalb der OMZ lokalisiert ist.
Anammox-Stickstoff-Isotopeneffekte entschlüsselt
Ein Wissenschaftlerteam des Max-Planck-Instituts für Marine Mikrobiologie, der Universität Basel und der Radboud Universität Nijmegen hat entscheidende Details eines wichtigen mikrobiellen Prozesses aufgedeckt und leistet damit einen großen Beitrag zum Verständnis der Stickstoffbilanz in den Weltmeeren. Sie berichten darüber in der Fachzeitschrift Proceedings of the National Academy of Sciences, USA.
Jedes Lebewesen braucht Stickstoff zum Leben und Wachsen
Viele Organismen haben nicht die Fähigkeit, lebensnotwendigen Stickstoff direkt aus dem molekularen Stickstoff zu nutzen, der als gasförmiges N<sub>2 </sub> in der Atmosphäre vorkommt. Sie haben in ihren Zellen nicht die entsprechenden Werkzeuge zur Stickstoff-Fixierung und sind deshalb auf Stickstoffverbindungen wie Ammonium, Nitrit und Nitrat angewiesen, die von den sogenannten Stickstoff-fixierenden Organismen kommen. In der Natur reguliert daher die biologische Verfügbarkeit von fixiertem Stickstoff häufig die Primärproduktion. Deshalb sind Düngemittel oft reich an Stickstoffverbindungen.
Es gibt in der Umwelt eine Reihe von anderen mikrobiellen Prozessen, die fixierten Stickstoff zur Energiegewinnung nutzen und wieder zu gasförmigem molekularen Stickstoff (N<sub>2 </sub>) umwandeln. Wissenschaftler sprechen hier von einem Verlust an fixiertem Stickstoff, weil dabei der jeweilige Lebensraum wichtige Stickstoffverbindungen verliert und so die Primärproduktion eingeschränkt wird.
Die Prozesse, die zum Stickstoffverlust führen, laufen in verschiedenen Mikroorganismen ab, manche reduzieren Nitrat und Nitrit, manche oxidieren Ammonium. Andere Bakterien nutzen Nitrit und Ammonium, um daraus molekularen Stickstoff zu bilden: Diese anaerobe Oxidation von Ammonium ist unter dem Begriff Anammox bekannt.
Stickstoffverluste sind besonders stark in den Meeresgebieten ausgeprägt, in denen der im Wasser gelöste Sauerstoff fast komplett verbraucht wurde. Diese Zonen werden als Oxygen Minimum Zones (OMZ) bezeichnet. Wissenschaftliche Studien lassen befürchten, dass sich diese OMZ aufgrund des Klimawandels weiter ausbreiten werden. Das könnte zu weitreichenden Konsequenzen bei den Stickstoffverlusten und damit bei der Primärproduktion in den Ozeanen führen. Deshalb ist es wichtig zu wissen, welcher mikrobielle Prozess wie stark zu den gesamten Stickstoffverlusten beiträgt und wo dieser innerhalb der OMZ lokalisiert ist.
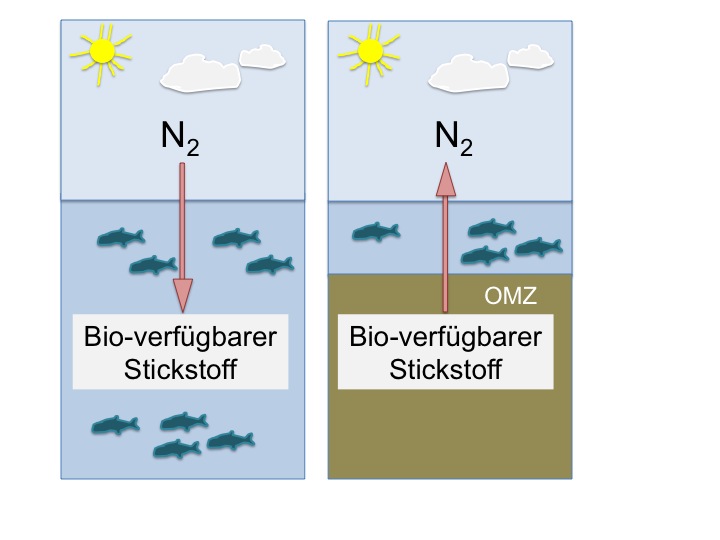
Schema zu den Stickstoffverlusten und -gewinnen in den Ozeanen
Links:
Stickstoffgas (N<sub>2</sub>) aus der Atmosphäre diffundiert in den Ozean und Mikroorganismen können diesen Stickstoff in Form von bioverfügbarem Stickstoff fixieren, der lebensnotwendig für alle Lebewesen ist.
Rechts:
In Gebieten mit Sauerstoffmangel (Oxygen Minimum Zones, OMZ) kann Anammox diesen fixierten Stickstoff wieder zu gasförmigen Stickstoff umwandeln und so Stickstoffverluste verursachen. Die neue Studie von Brunner et al entschlüsselt die Isotopeneffekte von Anammox, mit deren Hilfe verschiedenen Prozesse im Stickstoffkreislauf anhand der Isotopenverhältnisse von <sup>15</sup>N und <sup>14</sup>N in den Stickstoffreservoirs aller Stickstoffverbindungen verfolgt werden können. (Quelle Max-Planck-Institut für Marine Mikrobiologie.)
Links:
Stickstoffgas (N<sub>2</sub>) aus der Atmosphäre diffundiert in den Ozean und Mikroorganismen können diesen Stickstoff in Form von bioverfügbarem Stickstoff fixieren, der lebensnotwendig für alle Lebewesen ist.
Rechts:
In Gebieten mit Sauerstoffmangel (Oxygen Minimum Zones, OMZ) kann Anammox diesen fixierten Stickstoff wieder zu gasförmigen Stickstoff umwandeln und so Stickstoffverluste verursachen. Die neue Studie von Brunner et al entschlüsselt die Isotopeneffekte von Anammox, mit deren Hilfe verschiedenen Prozesse im Stickstoffkreislauf anhand der Isotopenverhältnisse von <sup>15</sup>N und <sup>14</sup>N in den Stickstoffreservoirs aller Stickstoffverbindungen verfolgt werden können. (Quelle Max-Planck-Institut für Marine Mikrobiologie.)
Bioreaktor mit einer Anreicherungskultur von Anammox. (Foto: Boran Kartal, Radboud Universität Nijmegen)
Gefunden: Das fehlende Teil zum Stickstoff-Puzzle
Prof. Dr. Benjamin Brunner, einer der Autoren, erklärt: ”Diese Frage können wir mithilfe der stabilen Stickstoffisotopen beantworten, indem wir die Mengenverhältnisse von <sup>15</sup>N und <sup>14</sup>N in den verschiedenen Reservoirs an fixiertem Stickstoff und im flüchtigen N<sub>2 </sub> bestimmten, denn die verschiedenen mikrobiellen Prozesse hinterlassen verschiedene Isotopenmuster. Manche dieser Reaktionen bevorzugen das leichtere <sup>14</sup>N vor dem schwereren <sup>15</sup>N, andere Prozesse ziehen das schwerere Isotop vor, Wissenschaftler bezeichnen diese Vorgänge als Isotopeneffekte.“
Dr. Sergio Contreras, ein Paleo-Biogeochemiker, der an der Vergangenheit und Zukunft des Stickstoffkreislaufes interessiert ist, ergänzt: ”Um die Stickstoff-Isotopenmuster in der Umwelt entschlüsseln zu können, muss man für alle Prozesse im Stickstoffkreislauf deren jeweilige Isotopeneffekte kennen.“
Prof. Dr. Moritz Lehmann, Isotopen-Biogeochemiker an der Universität Basel, sagt:
“Genau hier lag das Problem: Die Isotopeneffekte eines Prozesses, der mitverantwortlich für den Verlust an fixiertem Stickstoff ist, nämlich Anammox, waren bisher unbekannt. Es ist deshalb möglich, dass frühere wissenschaftliche Untersuchungen zu globalen Stickstoffverlusten falsch gewichtet und interpretiert wurden.“
Dr. Boran Kartal, Mikrobiologe an der Radboud University Nijmegen, erklärt: “Wir verwendeten für unsere Versuche hochangereicherte Anammox-Zellkulturen in unserem Labor, um deren Isotopeneffekte zu bestimmen. Unsere Ergebnisse belegen, dass die von Anammox verursachten Isotopeneffekte die Isotopenmuster in den OMZ, die sehr wichtig für die Primärproduktion sind, erklären können.”
Prof. Dr. Marcel Kuypers, Direktor am Max-Planck-Institut für Marine Mikrobiologie, fasst zusammen: ”Diese fehlende Information ist von größter Bedeutung zur Lösung des Stickstoff-Isotopen-Puzzles. Nicht nur, weil Anammox ein wesentlicher Prozess in den OMZ ist, sondern auch, weil Anammox die Isotopenzusammensetzung aller Stickstoff-Reservoirs beeinflusst: Es setzt Ammonium und Nitrit zu gasförmigem Stickstoff N<sub>2 </sub> und Nitrat um.”
Dank gemeinsamer Forschung gelang es den Wissenschaftlern, das komplizierte Isotopenmuster des Anammox-Prozesses zu entschlüsseln. Ihre Ergebnisse, die sie in den Proceedings of the National Academy of Sciences of the United States of America publizieren, erklären bisher seltsam erscheinende Isotopenmuster der OMZ und liefern das fehlende Teil des Stickstoff-Isotopen-Puzzles.
Weitere Informationen
Prof. Dr. Marcel Kuypers, +49 421 2028602, [Bitte aktivieren Sie Javascript]
Prof. Dr. Benjamin Brunner, +45 871 56586, [Bitte aktivieren Sie Javascript]
Dr. Gaute Lavik, +49 421 2028651, [Bitte aktivieren Sie Javascript]
Prof. Dr. Moritz Lehmann, [Bitte aktivieren Sie Javascript]
Dr. ir. Boran Kartal, [Bitte aktivieren Sie Javascript]
Pressesprecher
Dr. Manfred Schloesser, +49 421 2028704, [Bitte aktivieren Sie Javascript]
Originalpublikation
Nitrogen isotope effects induced by anammox bacteria
B. Brunner, S. Contreras, M.F. Lehmann, O. Matantseva, M. Rollog, T. Kalvelage, G. Klockgether, G. Lavik, M.S.M. Jetten, B. Kartal and M.M.M. Kuypers (2013)
Proc. Natl. Acad. Sci. USA, doi 10.1073/pnas.1310488110
Institute und Universitäten
Max-Planck-Institut für Marine Mikrobiologie, Abteilung Biogeochemie, Celsiusstraße 1, D-28359 Bremen
Departement Umweltwissenschaften (Biogeochemie), Universität Basel, Bernoullistrasse 30, 4056 Basel, Schweiz
Institute of Water and Wetland Research, Department of Microbiology, Radboud University Nijmegen, Heyendaelseweg 135, 6525 AJ Nijmegen, Die Niederlande
Prof. Dr. Benjamin Brunner, einer der Autoren, erklärt: ”Diese Frage können wir mithilfe der stabilen Stickstoffisotopen beantworten, indem wir die Mengenverhältnisse von <sup>15</sup>N und <sup>14</sup>N in den verschiedenen Reservoirs an fixiertem Stickstoff und im flüchtigen N<sub>2 </sub> bestimmten, denn die verschiedenen mikrobiellen Prozesse hinterlassen verschiedene Isotopenmuster. Manche dieser Reaktionen bevorzugen das leichtere <sup>14</sup>N vor dem schwereren <sup>15</sup>N, andere Prozesse ziehen das schwerere Isotop vor, Wissenschaftler bezeichnen diese Vorgänge als Isotopeneffekte.“
Dr. Sergio Contreras, ein Paleo-Biogeochemiker, der an der Vergangenheit und Zukunft des Stickstoffkreislaufes interessiert ist, ergänzt: ”Um die Stickstoff-Isotopenmuster in der Umwelt entschlüsseln zu können, muss man für alle Prozesse im Stickstoffkreislauf deren jeweilige Isotopeneffekte kennen.“
Prof. Dr. Moritz Lehmann, Isotopen-Biogeochemiker an der Universität Basel, sagt:
“Genau hier lag das Problem: Die Isotopeneffekte eines Prozesses, der mitverantwortlich für den Verlust an fixiertem Stickstoff ist, nämlich Anammox, waren bisher unbekannt. Es ist deshalb möglich, dass frühere wissenschaftliche Untersuchungen zu globalen Stickstoffverlusten falsch gewichtet und interpretiert wurden.“
Dr. Boran Kartal, Mikrobiologe an der Radboud University Nijmegen, erklärt: “Wir verwendeten für unsere Versuche hochangereicherte Anammox-Zellkulturen in unserem Labor, um deren Isotopeneffekte zu bestimmen. Unsere Ergebnisse belegen, dass die von Anammox verursachten Isotopeneffekte die Isotopenmuster in den OMZ, die sehr wichtig für die Primärproduktion sind, erklären können.”
Prof. Dr. Marcel Kuypers, Direktor am Max-Planck-Institut für Marine Mikrobiologie, fasst zusammen: ”Diese fehlende Information ist von größter Bedeutung zur Lösung des Stickstoff-Isotopen-Puzzles. Nicht nur, weil Anammox ein wesentlicher Prozess in den OMZ ist, sondern auch, weil Anammox die Isotopenzusammensetzung aller Stickstoff-Reservoirs beeinflusst: Es setzt Ammonium und Nitrit zu gasförmigem Stickstoff N<sub>2 </sub> und Nitrat um.”
Dank gemeinsamer Forschung gelang es den Wissenschaftlern, das komplizierte Isotopenmuster des Anammox-Prozesses zu entschlüsseln. Ihre Ergebnisse, die sie in den Proceedings of the National Academy of Sciences of the United States of America publizieren, erklären bisher seltsam erscheinende Isotopenmuster der OMZ und liefern das fehlende Teil des Stickstoff-Isotopen-Puzzles.
Weitere Informationen
Prof. Dr. Marcel Kuypers, +49 421 2028602, [Bitte aktivieren Sie Javascript]
Prof. Dr. Benjamin Brunner, +45 871 56586, [Bitte aktivieren Sie Javascript]
Dr. Gaute Lavik, +49 421 2028651, [Bitte aktivieren Sie Javascript]
Prof. Dr. Moritz Lehmann, [Bitte aktivieren Sie Javascript]
Dr. ir. Boran Kartal, [Bitte aktivieren Sie Javascript]
Pressesprecher
Dr. Manfred Schloesser, +49 421 2028704, [Bitte aktivieren Sie Javascript]
Originalpublikation
Nitrogen isotope effects induced by anammox bacteria
B. Brunner, S. Contreras, M.F. Lehmann, O. Matantseva, M. Rollog, T. Kalvelage, G. Klockgether, G. Lavik, M.S.M. Jetten, B. Kartal and M.M.M. Kuypers (2013)
Proc. Natl. Acad. Sci. USA, doi 10.1073/pnas.1310488110
Institute und Universitäten
Max-Planck-Institut für Marine Mikrobiologie, Abteilung Biogeochemie, Celsiusstraße 1, D-28359 Bremen
Departement Umweltwissenschaften (Biogeochemie), Universität Basel, Bernoullistrasse 30, 4056 Basel, Schweiz
Institute of Water and Wetland Research, Department of Microbiology, Radboud University Nijmegen, Heyendaelseweg 135, 6525 AJ Nijmegen, Die Niederlande